La Photobiomodulation : Décodage Biophysique de la Lumière Réparatrice et de son Impact sur le Vieillissement Cellulaire
Ce document d'expertise a été spécialement rédigé pour structurer et alimenter les épisodes du podcast "Fréquence Positive". En tant que vulgarisateur scientifique spécialisé en biophysique, l'objectif ici est de fournir une architecture narrative et factuelle d'une précision absolue (niveau de complexité 60-70/100). Nous allons plonger dans l'infiniment petit, là où les photons rencontrent la matière vivante, pour comprendre comment une exposition lumineuse non-ablative et athermique parvient à reprogrammer les horloges biologiques, à éteindre l'inflammation silencieuse et à restaurer l'intégrité de nos cellules.
11/20/202529 min read


Pendant des décennies, la biologie clinique a cantonné la lumière à deux fonctions élémentaires : un outil de la vision au niveau de la rétine, et un vecteur d'énergie thermique capable d'inciser ou d'abraser les tissus en chirurgie. Cependant, la biophysique moderne nous révèle une réalité bien plus fascinante, presque végétale : le corps humain interagit avec la lumière de manière photochimique, s'apparentant à une forme de photosynthèse humaine. Ce domaine de pointe est la Photobiomodulation (PBM), historiquement désignée dans la littérature sous le terme de Low-Level Laser/Light Therapy (LLLT).1
L'histoire de cette discipline débute de manière fortuite en 1967. Le chercheur hongrois Endre Mester, travaillant à l'Université médicale Semmelweis, tentait de reproduire des expériences de destruction tumorale à l'aide des tout premiers lasers à rubis récemment inventés (Mester et al., 1967, Semmelweis Medical University).1 Son laser, possédant une puissance dérisoire par rapport aux modèles américains de l'époque, échoua totalement à détruire les tumeurs implantées chez des rongeurs. Toutefois, Mester fit une observation qui allait bouleverser la médecine régénérative : la lumière de son laser à faible puissance, bien qu'incapable de chauffer ou de détruire, accélérait de manière spectaculaire la repousse des poils et la cicatrisation des incisions chirurgicales chez ces mêmes animaux.1 Ce fut la découverte de la "biostimulation laser", aujourd'hui rebaptisée photobiomodulation pour refléter sa capacité à moduler (stimuler ou inhiber selon la dose) les processus biologiques par la lumière.1
Aujourd'hui, les données extraites exclusivement de méta-analyses, d'études cliniques randomisées et de revues de littérature indexées sur PubMed, NCBI, Cochrane et publiées dans des revues phares comme Nature ou The Lancet, démontrent que la PBM opère bien au-delà de la simple cicatrisation cutanée. En utilisant des longueurs d'onde précises (typiquement entre 600 et 1100 nanomètres, englobant le rouge et le proche infrarouge), cette thérapie s'attaque aux fondements mêmes de la sénescence cellulaire, du déclin mitochondrial et de l'inflammaging.3
Ce rapport propose une exploration anatomique, métabolique et biophysique des mécanismes de la photobiomodulation. Nous allons disséquer comment un simple grain de lumière (le photon) parvient à réinitialiser le métabolisme, à préserver le capital génétique et à offrir une alternative douce et préservatrice face aux thérapies thermiques destructrices.
1. La Machinerie Quantique : Interactions entre Photons et Mitochondries
Pour saisir l'intelligence du corps en réponse à la lumière, il faut observer la cellule comme une ville complexe dont les mitochondries seraient les centrales électriques. L'énergie qui alimente chaque processus de la vie cellulaire — de la contraction d'une fibre musculaire à la transmission d'un signal nerveux — est stockée dans une molécule universelle : l'adénosine triphosphate (ATP). Avec le vieillissement et sous l'effet de maladies chroniques, ces centrales électriques s'encrassent, leur rendement chute, et la cellule entre dans un état de carence énergétique qui précipite sa dégénérescence.5
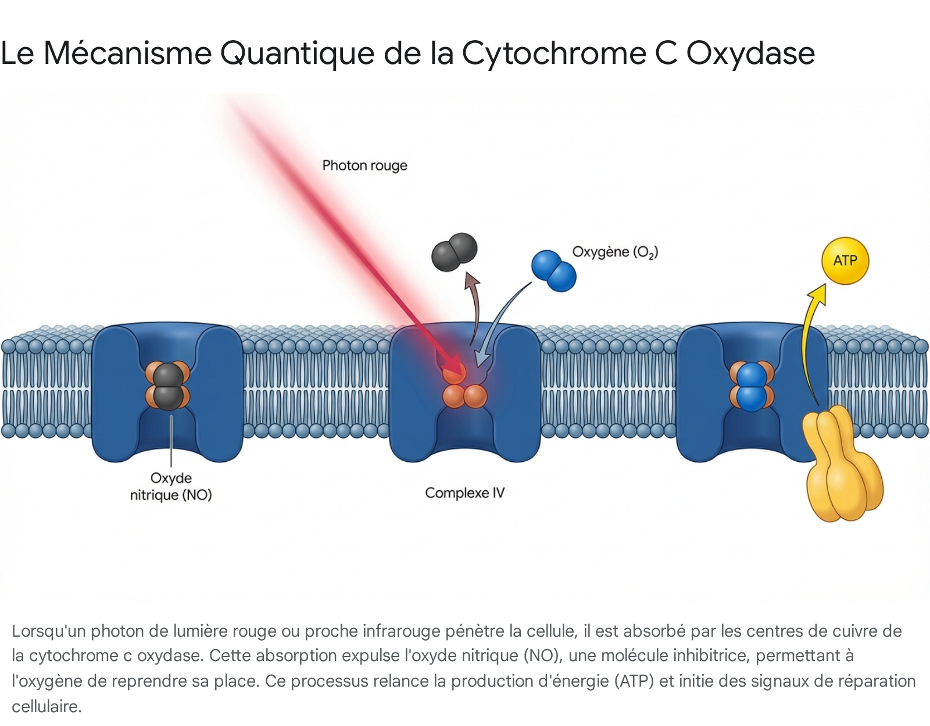
1.1. L'Antenne Photoréceptrice : La Cytochrome C Oxydase (CCO)
La photobiomodulation n'agit pas au hasard ; elle possède des cibles moléculaires très spécifiques appelées chromophores. Dans la plage des longueurs d'onde allant de 600 à 900 nanomètres, le principal chromophore cellulaire est la Cytochrome C Oxydase (CCO) (Karu, 1999, Journal of Photochemistry and Photobiology B: Biology).6
La CCO est une immense protéine transmembranaire qui constitue l'enzyme terminale (le Complexe IV) de la chaîne de transport d'électrons, située sur la membrane interne de la mitochondrie.7 Son rôle métabolique est critique : elle médie le transfert final des électrons du cytochrome c vers l'oxygène moléculaire ($O_2$), ce qui permet de pomper des protons à travers la membrane et de générer le gradient électrochimique indispensable à la synthèse d'ATP par l'ATP synthase.7
L'architecture moléculaire de la CCO est fascinante. Elle contient plusieurs centres métalliques, notamment des atomes de cuivre (CuA et CuB) et de fer héminique (hème a et hème a3).9 Les nuages électroniques de ces centres métalliques sont biophysiquement "accordés" pour absorber l'énergie des photons rouges et proches infrarouges (Hamblin, 2018, Photochemistry and Photobiology).11 Lorsqu'un photon frappe ces centres métalliques, son énergie est absorbée et entraîne une excitation électronique locale, modifiant l'état d'oxydoréduction de l'enzyme et déclenchant un changement conformationnel de sa structure tridimensionnelle.10
1.2. Lever le Frein Métabolique : La Photodissociation de l'Oxyde Nitrique
C'est ici que l'impact antivieillissement de la lumière prend tout son sens. Dans un tissu vieillissant, fatigué, blessé ou soumis à un stress pathologique, un phénomène pernicieux se produit. Une molécule de signalisation omniprésente, l'oxyde nitrique (NO), est produite en excès par les synthases d'oxyde nitrique mitochondriales (mtNOS).9
Bien que le NO soit vital pour la vasodilatation des vaisseaux sanguins, sa surabondance à l'intérieur de la mitochondrie est toxique. Le NO se lie de manière compétitive aux mêmes centres de cuivre (hème a3/CuB) de la CCO que l'oxygène moléculaire (Poyton et al., 2011, Discovery Medicine).13 Pour utiliser une métaphore simple, si l'oxygène est le carburant légitime de la centrale électrique, le NO agit comme un bouchon ou un "frein à main" serré à fond. Il bloque la chaîne de transport des électrons, provoque l'effondrement du potentiel de la membrane mitochondriale, stoppe la consommation d'oxygène et paralyse la production d'ATP.5
L'ingéniosité absolue de la photobiomodulation réside dans sa capacité physique à lever ce frein. L'excitation électronique provoquée par l'absorption des photons rouges et infrarouges a pour effet direct de photodissocier la liaison entre l'oxyde nitrique inhibiteur et la CCO.5 Sous l'impact de la lumière, le NO est littéralement éjecté de son site de liaison.
Une fois ce verrou sauté, l'oxygène moléculaire peut immédiatement reprendre sa place légitime. Le flux d'électrons est instantanément restauré, la consommation d'oxygène remonte en flèche, le gradient de protons est rétabli, et l'ATP synthase recommence à tourner à plein régime pour inonder la cellule de nouvelles molécules d'ATP.12
Ce réveil métabolique est particulièrement pertinent pour les organismes vieillissants. Des données présentées lors d'un atelier scientifique organisé par le National Institute on Aging (NIA) en janvier 2023 ont mis en évidence que les adultes plus âgés présentent typiquement une activité plus faible de la CCO et une connectivité fonctionnelle réduite au niveau systémique.5 Lors d'un essai clinique randomisé sur des adultes âgés de 18 à 85 ans utilisant un laser infrarouge à 1064 nm, les chercheurs ont constaté que la PBM augmentait significativement les niveaux de CCO oxydée et d'hémoglobine oxygénée.5 De manière cruciale, cette étude a démontré que l'effet amplificateur sur la CCO était d'autant plus grand que l'âge des participants était avancé. La lumière agit donc de manière compensatoire : elle offre son potentiel maximal précisément là où le déclin mitochondrial lié à l'âge est le plus sévère, ouvrant des perspectives majeures pour la neuroprotection et le maintien de la vitalité systémique.5
1.3. La Cascade de Signalisation : Du Second Messager au Noyau
L'augmentation spectaculaire de l'ATP n'est pas une fin en soi ; elle agit comme la première dominos d'une longue chaîne de commandement. L'élévation des niveaux d'ATP entraîne sa conversion rapide en adénosine monophosphate cyclique (AMPc) par l'enzyme adénylate cyclase.15
L'AMPc est ce qu'on appelle en biologie un "second messager" intracellulaire ubiquitaire. Sa présence indique à la cellule qu'elle dispose de l'énergie nécessaire pour passer d'un état de simple survie végétative à un état de reconstruction active. L'AMPc va notamment activer des protéines kinases majeures, comme la Protéine Kinase A (PKA) et la voie Ras, qui se propagent ensuite pour activer d'autres voies de signalisation fondamentales comme la SIRT1 et la voie ERK (Extracellular signal-regulated kinases).15
Ce dialogue biochimique qui naît dans la mitochondrie (sous l'impulsion de la lumière) et voyage à travers le cytoplasme pour finalement dicter ses ordres au noyau de la cellule est appelé signalisation mitochondriale rétrograde (Karu, 1999).6 Par le biais de cette signalisation, de simples photons réussissent l'exploit de modifier l'expression génétique de la cellule. Ils commandent au noyau d'activer une vaste gamme de facteurs de transcription qui conduisent à une amélioration de la survie cellulaire, à une prolifération accrue, à la migration (essentielle pour refermer les plaies) et à la synthèse de protéines réparatrices inédites (HSP-60, VEGF, HIF-1α) tout en bloquant l'expression des gènes responsables de la mort cellulaire (apoptose).5
1.4. L'Alternative des Canaux Ioniques Membranaires
Il est crucial de préciser que si la Cytochrome C Oxydase règne en maître sur l'absorption de la bande allant de 600 à environ 850 nm, d'autres acteurs prennent le relais pour les longueurs d'onde supérieures du proche infrarouge (notamment de 980 à 1064 nm). En effet, l'absorption lumineuse de la CCO s'effondre au-delà d'un certain seuil.9
Dans ces registres de fréquences plus profondes, la littérature (indexée sur PubMed et issue de publications comme Oxidative Medicine and Cellular Longevity, 2017) pointe vers l'implication de structures logées directement dans la membrane cellulaire extérieure : les canaux ioniques sensibles à la lumière et à l'infime chaleur métabolique locale.5
Il s'agit tout particulièrement des canaux de la famille TRP (Transient Receptor Potential), couplés à des molécules photoréceptrices comme les opsines (Nayak et al., 2020, Cell Rep.).9 Lorsque ces longueurs d'onde ciblent la cellule, elles provoquent un changement de perméabilité transitoire au niveau de ces canaux. Le résultat immédiat est un influx massif et parfaitement chorégraphié d'ions calcium ($Ca^{2+}$), de sodium et de magnésium de l'extérieur vers l'intérieur de la cellule.5
Ce pic de calcium intracellulaire est un puissant déclencheur métabolique. Il influe sur le traitement des récepteurs couplés aux protéines G (GPCR). Des études ont mis en évidence des actions extrêmement ciblées de cette dynamique : par exemple, la stimulation des canaux TRPV4 dans les cellules ganglionnaires de la rétine déclenche des potentiels membranaires vitaux, tandis que l'action sur les récepteurs TRPV2 dans les mastocytes module finement la réponse immunitaire (Savina et al., 2003, J Biol Chem.).5 La photobiomodulation possède donc un double mécanisme d'action : elle agit comme un interrupteur chimique (via la mitochondrie et la CCO) et comme un interrupteur électrophysiologique (via les canaux ioniques et le calcium), élargissant considérablement son spectre thérapeutique.5
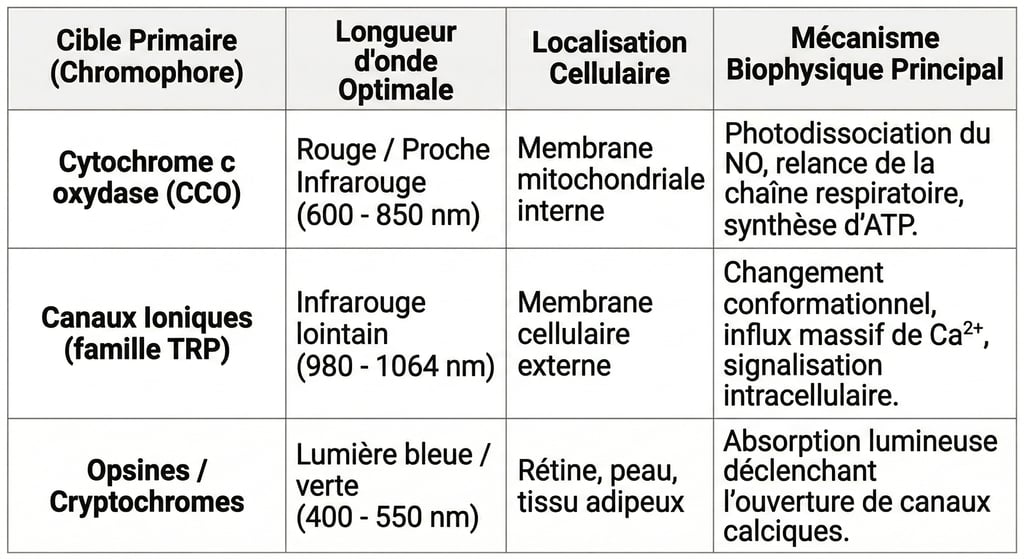
Tableau récapitulatif des principales cibles cellulaires interagissant avec différentes longueurs d'onde lumineuses.
2. Le Paradoxe Hormétique : Maîtriser le Stress Oxydatif pour Protéger la Cellule
Un aspect particulièrement mal compris dans la vulgarisation scientifique grand public est le rapport entre la photobiomodulation et le stress oxydatif. Historiquement, le grand récit anti-âge a diabolisé les Espèces Réactives de l'Oxygène (ROS), souvent vulgarisées sous le terme de "radicaux libres". Ces molécules instables, possédant des électrons non appariés, étaient perçues uniquement comme des agents de destruction, oxydant les lipides, dénaturant les protéines et brisant l'ADN, causant le vieillissement inéluctable de nos tissus.
La biophysique actuelle nous oblige à adopter une perspective beaucoup plus nuancée. Les ROS ne sont pas de simples "déchets" métaboliques ; ce sont également de puissants messagers biologiques de première ligne. La relation entre la lumière, les radicaux libres et la guérison repose sur un concept fondamental en toxicologie que la PBM exploite avec une élégance rare : l'hormèse.
2.1. L'Éclat de ROS : Un Mimétique de l'Exercice Physique
Lorsqu'une cellule saine et au repos (quiescente) est exposée à la photobiomodulation, l'accélération subite de la chaîne de transport d'électrons mitochondriale engendre une "fuite" inévitable d'électrons mineure. Cette fuite produit un bref, transitoire, mais mesurable éclatement de ROS (principalement des superoxydes) (Hamblin, 2018).11
Loin d'être destructeur, ce micro-stress oxydatif agit comme un signal d'alarme adaptatif ou un "eustress" (un bon stress). Biologiquement, ce bref pic de ROS provoqué par la lumière rouge et proche infrarouge imite presque parfaitement la signature biochimique que la cellule expérimente lors d'un exercice physique intense (exercise mimetic).16
Pour faire face à cette alerte perçue, la cellule va déployer un arsenal défensif massif et disproportionné par rapport à l'insulte initiale. Le pic transitoire de ROS active des facteurs de transcription majeurs de survie cellulaire. Le plus important d'entre eux est le complexe Nrf2 (Nuclear factor erythroid 2-related factor 2).14 Sous l'effet du signal photonique, le Nrf2 se détache de son inhibiteur dans le cytoplasme et voyage (se transloque) vers le noyau de la cellule. Là, il se lie à l'Élément de Réponse Antioxydant (ARE) de l'ADN, ordonnant instantanément la transcription et la synthèse massive de notre propre pharmacopée antioxydante endogène (Ding et al., 2016).18
En réponse à une exposition lumineuse, la cellule inonde son propre milieu d'enzymes surpuissantes telles que la Superoxyde Dismutase (SOD), la catalase et les systèmes liés au glutathion, renforçant considérablement l'armure cellulaire contre les véritables agressions futures.14
2.2. L'Effet Bouclier sur les Cellules Pathologiques
L'intelligence profonde de ce mécanisme se révèle pleinement lorsque l'on observe l'action de la lumière sur des cellules malades, vieillissantes ou déjà en état de détresse oxydative. Dans les modèles pathologiques (lésions cérébrales, ischémie, brûlures, dystrophies musculaires), le niveau de base des ROS est chroniquement et toxiquement élevé.4 Les systèmes de défense endogènes de la cellule sont submergés.
On pourrait logiquement craindre que l'application d'une thérapie qui génère des ROS (comme la PBM sur des cellules saines) ne vienne aggraver l'état d'une cellule déjà en stress oxydatif. Le miracle biophysique est que c'est l'exact inverse qui se produit. Lorsqu'elle est appliquée à des cellules soumises à un stress oxydatif sévère, la photobiomodulation abaisse de manière spectaculaire les niveaux globaux de ROS toxiques.14
Comment expliquer cette apparente contradiction? La réponse est double. Premièrement, le rétablissement fulgurant du potentiel de membrane mitochondrial par l'éviction de l'oxyde nitrique optimise le rendement de la chaîne respiratoire, colmatant les fuites excessives d'électrons responsables de la toxicité oxydative chronique.5 Deuxièmement, la surexpression salvatrice des défenses antioxydantes par la voie Nrf2 "nettoie" le surplus destructeur.
Une étude révélatrice a été menée sur des cellules musculaires isolées de souris mdx, le modèle animal de la dystrophie musculaire, une pathologie marquée par un niveau cataclysmique de dommages oxydatifs. Les chercheurs ont appliqué une lumière proche infrarouge à 830 nm (avec une densité d'énergie de 5 J/cm²).14 Les résultats ont démontré que la PBM réduisait non seulement la production de peroxyde d'hydrogène ($H_2O_2$) et les biomarqueurs cruciaux des dommages lipidiques par les radicaux libres (comme le 4-HNE et le TBARS), mais que, ce faisant, elle diminuait l'activité globale de la SOD et de la Glutathion Réductase dans ces cellules malades.14 La lumière a réparé la fonction métabolique fondamentale avec une telle efficacité que la cellule n'avait plus besoin de maintenir ses systèmes d'urgence enzymatique en état d'alerte permanente, lui permettant de réallouer son énergie vers la cicatrisation tissulaire.14
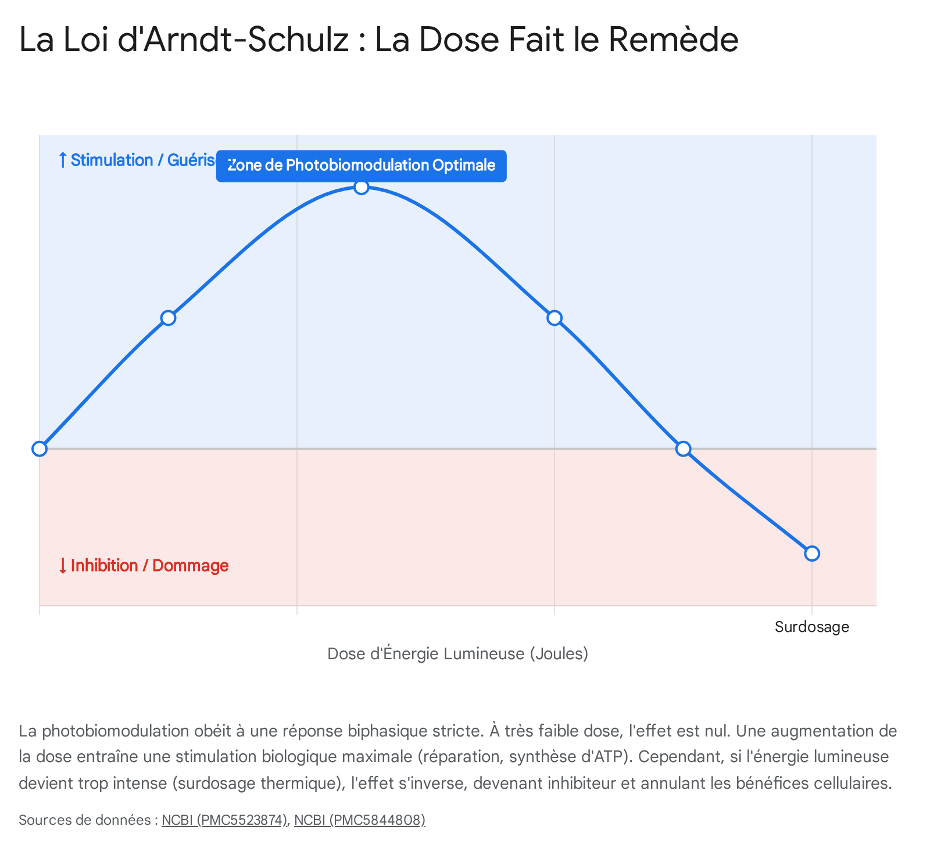
2.3. La Loi d'Arndt-Schulz : La Nécessité de la Douceur
Ce dialogue complexe avec les ROS explique la loi d'airain qui régit la photobiomodulation : la courbe de réponse biphasique (ou Loi d'Arndt-Schulz).16 Cette loi stipule que les effets biologiques de la lumière ne sont pas linéaires, mais obéissent à une courbe en forme de cloche (ou en "U" inversé).
Une très faible dose d'énergie lumineuse ne parvient pas à exciter la Cytochrome C Oxydase et n'induit aucun effet biologique.16 À mesure que la dose augmente (typiquement entre 2 et 10 Joules/cm², selon les tissus et la longueur d'onde), l'impact réparateur grimpe, la production d'ATP culmine et les facteurs de croissance sont déployés.9 C'est la zone de stimulation thérapeutique.
Toutefois, si l'opérateur continue d'augmenter la densité d'énergie ou la puissance d'irradiation pensant que "plus c'est mieux" (un biais humain très courant), les bénéfices commencent à chuter rapidement pour revenir au niveau de base.16 Pire encore, un surdosage d'énergie lumineuse crée un emballement oxydatif qui ne peut plus être géré par l'hormèse. La surabondance de photons sature la mitochondrie, générant un tsunami de ROS qui va inverser les effets : la thérapie devient inhibitrice, bloque le métabolisme et peut même endommager l'architecture tissulaire par un excès de chaleur ou de cytotoxicité (phototoxicité).16 La PBM exige donc une précision dosimétrique rigoureuse ; sa force réside paradoxalement dans sa douceur.
3. L'Inflammaging, les Cellules Zombies et la Reprogrammation Immunitaire
Au fil des décennies, notre corps accumule des erreurs de réplication, des débris protéiques et des dommages oxydatifs. Ce fardeau constant maintient notre système immunitaire dans un état d'alerte chronique, bas bruit et dysfonctionnel. Cette inflammation sourde, stérile (non causée par un agent pathogène) et persistante est appelée inflammaging (inflammation liée au vieillissement).17 L'inflammaging est aujourd'hui identifié comme le tronc commun de la majorité des maladies dégénératives, des maladies cardiovasculaires au déclin cognitif en passant par l'arthrose.17
La photobiomodulation s'affirme dans la littérature scientifique comme l'un des régulateurs non pharmacologiques les plus reproductibles et les plus puissants de l'inflammation tissulaire.14
3.1. Le Maître Régulateur : Le Facteur de Transcription NF-κB
Le chef d'orchestre de l'inflammation dans nos cellules est un complexe protéique appelé NF-κB (Nuclear factor kappa-light-chain-enhancer of activated B cells). L'analyse biophysique approfondie de l'action de la lumière sur ce facteur révèle à nouveau un effet "adaptogène" et éminemment contextuel.14
Dans des fibroblastes embryonnaires sains ou des cellules musculaires saines, la PBM utilise les transitoires ROS pour activer de manière éphémère le NF-κB, l'utilisant comme un interrupteur de prolifération cellulaire favorisant la croissance et la viabilité des tissus jeunes.14
À l'inverse, dans des cellules plongées dans un chaos inflammatoire (comme des synoviocytes issus de patients atteints de polyarthrite rhumatoïde stimulés au préalable par des marqueurs inflammatoires, ou dans des modèles in vivo de traumatismes de la moelle épinière), la PBM orchestre un retrait stratégique spectaculaire.14 L'exposition à la lumière rouge/proche infrarouge (par exemple à 810 nm, de 5 à 25 J/cm²) entraîne une chute drastique de l'expression des ARN messagers et des protéines du complexe NF-κB (Basso et al., 2015, Photochemistry and Photobiology).6
En bloquant cette voie maîtresse, la lumière assèche la production à la source des pires acteurs de l'inflammation. Les méta-analyses documentent des diminutions impressionnantes des cytokines pro-inflammatoires majeures : le Facteur de Nécrose Tumorale alpha (TNF-α), l'Interleukine-1β (IL-1β), l'Interleukine-6 (IL-6, un marqueur clé de l'inflammaging et de l'atteinte de la longévité), l'Interleukine-8 (IL-8) ainsi que des métabolites douloureux comme la prostaglandine E2 (PGE2).14 Parallèlement, des rapports montrent que la PBM augmente la synthèse des résolvines et des protectines, des molécules dérivées des acides gras oméga-3 dont la seule fonction biologique est de résoudre l'inflammation aiguë et d'accélérer la cicatrisation tissulaire.14
3.2. Repolarisation des Macrophages : Changer les Armes en Outils
Pour soutenir un état inflammatoire chronique, le corps mobilise des bataillons de cellules immunitaires appelées macrophages. En temps de crise aiguë (une infection, une coupure), ces macrophages adoptent un phénotype dit "M1" : ils sont agressifs, libèrent du peroxyde et détruisent tout sur leur passage pour éradiquer l'agent pathogène.14 Une fois le travail terminé, ils sont censés se transformer en phénotype "M2", des macrophages paisibles qui nettoient les débris et sécrètent des facteurs de croissance pour réparer le tissu blessé.14 Dans le vieillissement, cette transition s'enraye, et les macrophages restent bloqués en phase M1, s'attaquant aux tissus sains.
L'énergie photonique agit comme un signal de pacification irrésistible. L'irradiation de macrophages activés de type M1 (stimulés par interférons et lipopolysaccharides) avec des longueurs d'onde de 660 nm et 780 nm réduit physiquement l'expression génétique des marqueurs d'agressivité (comme l'enzyme iNOS et le gène chimiotactique CCL3).14 La PBM force la repolarisation des cellules immunitaires, éteignant l'agressivité stérile (réduction de l'expression des marqueurs CD86 et du complexe majeur d'histocompatibilité de classe II sur les cellules dendritiques) pour faire basculer le tissu dans une phase de reconstruction et d'angiogenèse (formation de nouveaux vaisseaux sanguins).14
3.3. Le Phénotype Sécrétoire Associé à la Sénescence (SASP)
L'une des plus grandes découvertes récentes en géroscience, discutée dans des revues phares comme Nature Reviews Molecular Cell Biology (Campisi, 2007) 26, est la notion de "cellules sénescentes". Lorsqu'une cellule subit trop de stress (ADN endommagé, télomères trop courts), au lieu de s'autodétruire proprement (apoptose), elle entre parfois dans un état "zombie".27 Elle arrête de se diviser mais refuse de mourir, et commence à polluer son environnement.
Ce comportement toxique est nommé le Phénotype Sécrétoire Associé à la Sénescence (SASP).26 Ces cellules zombies déversent des quantités colossales de cytokines pro-inflammatoires (IL-6, IL-8), de facteurs de croissance aberrants et de métalloprotéinases qui dégradent la matrice extracellulaire saine, convertissant les cellules voisines en zombies à leur tour et favorisant des microenvironnements propices à la tumorigenèse (Campisi, 2007 ; Van Deursen, 2014).26
La recherche pharmaceutique moderne tente de créer des "sénolytiques" pour tuer chimiquement ces cellules.26 La photobiomodulation, fidèle à son approche de préservation tissulaire, adopte une stratégie "sénomorphique".26 Sans tuer la cellule sénescente de manière indiscriminée, la lumière modifie le profil de ses sécrétions. En ciblant des marqueurs du cycle cellulaire comme p16, p21 et p53, la PBM parvient à supprimer les composants inflammatoires dévastateurs du SASP tout en conservant intacts les signaux réparateurs indispensables à la régénération, évitant ainsi le risque d'immunosuppression tissulaire souvent associé aux approches destructrices.11
3.4. Le Réseau Redox-Médié NF-κB – TGF-β1 – ATF-4
Les recherches de pointe en biophysique, synthétisées dans Lasers in Medical Science, ont récemment mis en évidence l'existence d'un axe de signalisation extracellulaire somptueux initié par la PBM : l'axe Redox-Médié NF-κB – TGF-β1 – ATF-4.21
Lorsque le très léger nuage de ROS (créé initialement dans la mitochondrie par l'impact du photon) diffuse à travers la membrane vers le milieu extracellulaire (la matrice interstitielle), il rencontre une protéine essentielle en sommeil : le Facteur de Croissance Transformant bêta-1 latent (Latent TGF-β1).5 Ce facteur de croissance flotte dans un état inactif, maintenu prisonnier par un peptide. Le très fin signal redox de la lumière cible spécifiquement un acide aminé de ce peptide (la méthionine sensible à l'oxydation en position 253), modifiant instantanément sa forme et libérant la forme active et puissante du dimère TGF-β1.5
Ce facteur de croissance activé par la lumière s'attache ensuite aux récepteurs cellulaires environnants, enclenchant l'expression du Facteur de Transcription Activant 4 (ATF-4), à la fois par des voies canoniques (les protéines Smad2 et Smad3) et non-canoniques (p38 et ERK).21 L'ATF-4 est le chef de chantier suprême de la survie cellulaire face au stress : il bloque la destruction cellulaire, ordonne le recyclage des protéines mal repliées ou toxiques (via une autophagie contrôlée impliquant les protéines de choc thermique HSP), et force la différenciation des cellules souches hôtes pour régénérer physiquement le tissu (tissu osseux, cartilage, épiderme).5
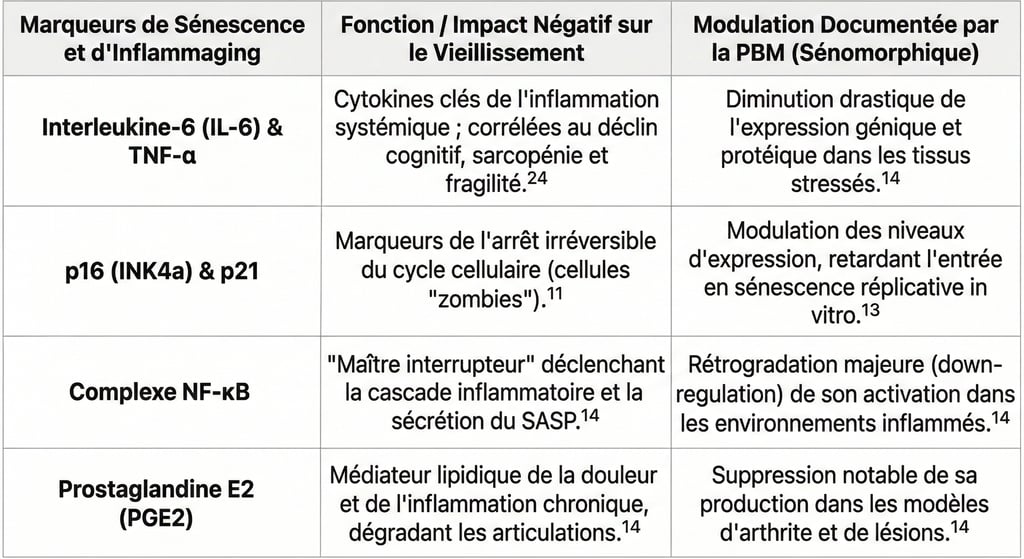
Récapitulatif de l'action sénomorphique et anti-inflammatoire de la photobiomodulation.
4. Télomères, Sirtuines et le Sablier du Vieillissement
L'une des horloges biologiques les plus documentées du vieillissement humain est l'usure de nos télomères (Varadhan et al., 2016, J. Am. Geriatr.).32 Ce sont des séquences répétitives d'ADN (TTAGGG) situées à l'extrémité de chaque chromosome, agissant comme des embouts en plastique de lacets pour empêcher l'ADN de s'effilocher.33 À chaque fois qu'une cellule somatique se divise, ces télomères se raccourcissent légèrement. Lorsqu'ils atteignent une taille critique, la cellule ne peut plus se diviser, déclenchant une alerte aux dommages de l'ADN conduisant inexorablement à l'arrêt du fonctionnement organique et à l'attrition tissulaire (syndromes neurodégénératifs, fibroses, défaillances des cellules souches).33
La perspective d'utiliser une source d'énergie électromagnétique inoffensive pour intervenir sur ces structures nucléaires semblait relever de la science-fiction, jusqu'à l'avènement des analyses biophysiques et génétiques modernes.
4.1. Préservation du Complexe Shelterine et de l'Architecture Télomérique
L'ADN télomérique nu serait extrêmement vulnérable. Pour le protéger, la cellule fabrique un bouclier protéique complexe appelé le complexe Shelterine, composé de six protéines, dont TRF1, TRF2, TIN2, POT1, TPP1, et RAP1.34
Les données expérimentales soulignent que la lumière proche infrarouge de basse puissance est capable de moduler directement la stabilité de ce bouclier. Dans des modèles expérimentaux sévères imitant les conditions d'un sepsis aigu causant de graves lésions pulmonaires (ALI - Acute Lung Injury) chez l'animal, le choc inflammatoire systémique entraîne un raccourcissement brutal des télomères dans les tissus cardiaques et un effondrement des niveaux de la protéine protectrice TRF1.35
L'irradiation des tissus affectés par un laser infrarouge à faible puissance (avec une densité d'énergie modérée de 10 J/cm²) a permis non seulement de stopper la dégradation, mais de provoquer une augmentation statistiquement significative de la longueur relative des télomères dans ces cellules cardiaques stressées.35 L'analyse moléculaire suggère que la lumière maintient l'intégrité télomérique non pas nécessairement en augmentant aveuglément TRF1 dans les tissus malades, mais en stabilisant les interactions entre d'autres composants clés de la shelterine (comme le sous-complexe TIN2 couplé à POT1/TPP1).35 Plus fascinant encore, la lumière semble faciliter la processivité de la télomérase, la seule enzyme capable de rajouter matériellement des séquences de nucléotides aux extrémités chromosomiques pour rallonger la vie cellulaire.35
Des résultats corroborants obtenus sur des fibroblastes dermiques humains en culture ont confirmé que l'application de paramètres PBM appropriés (à 590 nm notamment) retardait de manière univoque l'attrition des télomères et l'entrée dans la sénescence réplicative, constituant un effet antivieillissement intrinsèque induit par la lumière (Étude publiée dans Photomedicine and Laser Surgery, 2020).30
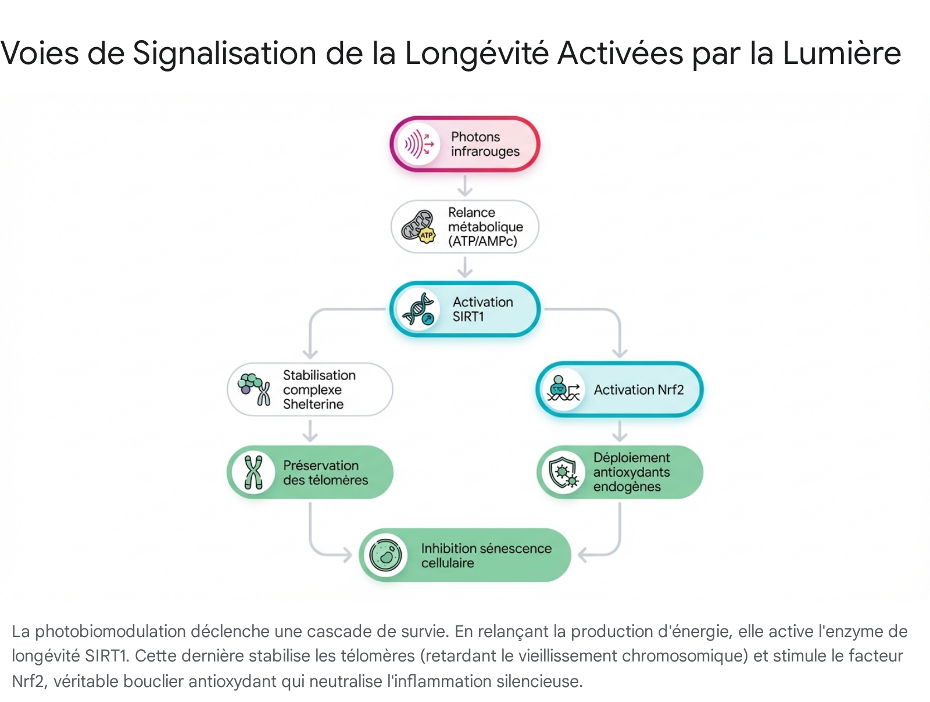
4.2. L'Enzyme de Longévité SIRT1 : Fermer la Boucle Antioxydante
Pour compléter ce portrait du rajeunissement moléculaire, la recherche montre que les dommages et le raccourcissement télomériques entraînent l'effondrement des niveaux cellulaires des Sirtuines, via une régulation négative menée par la protéine p53 et de multiples micro-ARN.34 Les Sirtuines (dont les SIRT1 à SIRT7) sont une famille fascinante de désacétylases dépendantes du NAD+, connues sous le nom d'"enzymes de longévité", agissant comme des capteurs de nutriments et régulant étroitement la santé métabolique et mitochondriale.34 Au cours du vieillissement normal, dans des échantillons de cellules souches mésenchymateuses osseuses, on constate une baisse de près de 7,2 fois de l'expression de SIRT1 chez les donneurs âgés par rapport aux jeunes.13
La photobiomodulation agit comme un remède d'exception face à ce déclin. En induisant la cascade AMPc et l'activation de la Protéine Kinase A au niveau des mitochondries, l'exposition à la lumière déclenche une régulation à la hausse massive de l'activité de l'enzyme SIRT1.16
Cette augmentation artificielle de la SIRT1 par la lumière produit des effets de cascade stupéfiants. D'une part, SIRT1 surexprimée stimule directement la voie Nrf2 (le facteur de transcription des défenses antioxydantes décrit plus haut), complétant et renforçant la boucle de protection contre le stress oxydatif.18 D'autre part, la SIRT1 induit elle-même des mécanismes de réparation de l'ADN et favorise l'expression de l'hTERT (le composant catalytique de la télomérase), protégeant physiquement le génome (Dhillon et al., Biol. Reprod.).36
Des travaux majeurs, publiés dans le très prestigieux journal Aging Cell en 2019, ont démontré que dans des modèles de la maladie d'Alzheimer (souris transgéniques accumulant des plaques amyloïdes toxiques), la photobiomodulation s'appuyait spécifiquement sur cette activation de SIRT1 pour protéger les neurones (Zheng et al., Neuroscience ; Banerjee et al., Int J Alzheimers Dis.).15 La lumière, via SIRT1, parvient à orienter le traitement de la protéine précurseur de l'amyloïde vers une voie saine non amyloïdogène, augmentant la production d'ADAM10 et inhibant BACE1.19 Le résultat net est une réduction spectaculaire de la formation des plaques Aβ et une amélioration tangible des capacités cognitives et de la mémorisation.19 Ces résultats extraordinaires soulignent que la lumière est capable de dicter un comportement de résilience face à des pathologies dégénératives structurelles parmi les plus graves.4
5. De la Rétine à la Boîte Crânienne : Applications Cliniques et Perspectives
Les mécanismes biophysiques décrits jusqu'ici (relance de l'ATP, levée du frein NO, signalisation par les ROS et SIRT1, sauvegarde de l'ADN, maîtrise de l'inflammaging) font de la photobiomodulation un outil d'une polyvalence clinique extraordinaire, ciblant des organes complexes allant bien au-delà de la peau.
5.1. Neuroprotection et Transcranial Photobiomodulation (tPBM)
L'un des organes vitaux les plus riches en mitochondries et les plus gourmands en oxygène (et donc en ATP) est le cerveau humain. Il est par conséquent extrêmement sensible au déclin mitochondrial induit par l'âge et au stress oxydatif, fondements des troubles allant de l'anxiété aux démences neurodégénératives (Alzheimer, Parkinson) et aux ischémies (AVC).4
La barrière protectrice du crâne n'est pas un obstacle absolu. La lumière, en particulier dans le spectre proche infrarouge (aux alentours de 800 à 1064 nm), possède des propriétés physiques d'absorption et de diffusion qui lui permettent de traverser la peau, l'os crânien, et de pénétrer dans le tissu cérébral sur une profondeur estimée jusqu'à 20 mm sous la surface corticale.4 L'application de dispositifs d'irradiation sur la tête (via des casques intégrant des matrices de LEDs) porte le nom de Photobiomodulation Transcrânienne (tPBM).4
Les études documentent que la tPBM augmente localement le débit sanguin cérébral, l'oxygénation de l'hémoglobine, relance la machinerie cytochrome c oxydase des neurones corticaux fatigués, tout en déployant des facteurs neurotrophiques et en bloquant l'inflammation de la microglie.4 L'exploration de ces effets lors de l'atelier du National Institute on Aging (NIA) confirme que ces signaux rétrogrades offrent de profonds effets neuroprotecteurs et améliorent les déficits cognitifs chez des modèles animaux et dans de premiers essais de phase 2 chez l'homme.5
5.2. Santé Systémique, Rétine et Atteintes Musculaires
En ophtalmologie, la Rétine, tissu nerveux d'une densité métabolique inégalée, souffre d'inflammaging, conduisant à la Dégénérescence Maculaire Liée à l'Âge (DMLA).12 L'application de la PBM réduit les marqueurs spécifiques du stress glial (vimentine et protéine GFAP) et inhibe l'hyperactivation du système du complément immunitaire, suggérant un frein réel à la mort des photorécepteurs.12
Sur le plan de la longévité systémique et cardiovasculaire, des études longitudinales de pointe (employant des ondes infrarouges de 850 nm sur des modèles animaux à un âge très avancé) ont révélé que la thérapie restaurait significativement l'épaisseur de la paroi ventriculaire gauche (LVWT), améliorait la dimension de l'oreillette gauche et optimisait la vitesse de l'onde de pouls (PWV), un marqueur critique de la rigidité et de la jeunesse artérielle (Knoops et al., JAMA ; Drew et al., Hemodial Int.).5
Enfin, la PBM est devenue un outil de récupération physique systémique. Même chez les patients en Unités de Soins Intensifs (USI), une exposition lumineuse ciblée a démontré, selon des travaux publiés dans le Journal of Biophotonics (2024), une diminution du temps de séjour de près de 30 %, accompagnée d'une amélioration foudroyante de la mobilité (passant de 110% à 255% sur l'échelle IMS) et de la force de préhension, neutralisant littéralement l'atrophie musculaire par la signalisation mitochondriale et antioxydante.40
6. La Frontière Biologique Absolue : Stimulation Douce vs Destructions Thermiques
Devant la myriade de bénéfices cliniques, une confusion intellectuelle et marketing massive perdure dans les domaines du bien-être et du médical : la distinction entre les thérapies lumineuses "douces" (PBM) et les interventions au "laser" de puissance utilisées en kinésithérapie, en chirurgie, ou en esthétique.3
Historiquement, le seul nom de "laser" (inventé pour la découpe, l'ablation et l'armement) suggérait un effet destructeur ou incisif. La littérature scientifique classe rigoureusement les interactions lumière/tissu en trois taxonomies basées sur l'énergie délivrée et la vitesse de dépôt de cette énergie. Il est fondamental d'établir que les mécanismes cellulaires de la photobiomodulation n'ont biologiquement rien à voir avec les autres techniques utilisant de la lumière.42
6.1. La Triade des Effets Optiques sur le Vivant
1. L'Effet Photochimique (PBM / LLLT - Low-Level Laser Therapy) : C'est l'apanage exclusif de la photobiomodulation que nous avons explorée jusqu'ici. Elle emploie des densités de puissance extrêmement basses (de l'ordre du milliwatt, typiquement entre 1 mW et 1 Watt) et une diffusion lente de l'énergie.3 Conséquence capitale : l'irradiation se fait en dessous du seuil thermique des tissus.3 L'absorption des photons par les chromophores (CCO, opsines, TRP) dicte une bio-stimulation purement biochimique. L'architecture cellulaire n'est soumise à aucune élévation de température, elle est préservée et "renseignée" au niveau génétique.43
2. L'Effet Photothermique (HPLT - High-Power Laser Therapy) : Ces systèmes thérapeutiques recourent à des lasers chirurgicaux ou physiothérapeutiques très puissants (allant de 1 à 10 Watts, soit des dizaines à des milliers de fois plus d'énergie par seconde qu'un appareil de PBM).3 L'objectif biomécanique change drastiquement : l'absorption brutale de cette énergie lumineuse par la mélanine et les molécules d'eau intracellulaires et extracellulaires est immédiatement convertie en chaleur locale intense (Ahrar et al., Lasers Med. Sci. ; Coleman et al., Photomed. Laser Surg.).43 Cette élévation de température force une vasodilatation immédiate et induit une dénaturation contrôlée et un remodelage des fibres de collagène. Cet effet est cliniquement valide pour la prise en charge immédiate d'une douleur musculaire profonde ou l'évaporation de tumeurs superficielles, mais il est par nature pro-inflammatoire et repose sur le principe d'une lésion thermique, causant du stress à la cellule.3
3. L'Effet Photoacoustique (True HILT - High-Intensity Laser Therapy) : C'est le royaume des impulsions lumineuses ultra-courtes, caractérisées par un rapport cyclique très faible (0,01 à 1%) mais une puissance crête titanesque dépassant le kiloWatt (kW) en une fraction de milliseconde.43 Cette énergie colossale percute le tissu à une telle vitesse qu'elle provoque une expansion thermoélastique instantanée de l'eau intracellulaire, générant une véritable onde de pression mécanique (des micro-ondes de choc).43 Ce processus de mécano-transduction force le cartilage ou la matrice osseuse profonde à se remodeler physiquement. C'est une interaction mécanique brutale, bien que salvatrice pour l'arthrose sévère, mais qui diffère totalement d'une conversation photochimique.42
Sources des citations
1. Photobiomodulation or low-level laser therapy - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC5215795/
2. Low-Level Light/Laser Therapy Versus Photobiomodulation Therapy - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC4390214/
3. Proposed Guidelines for Reporting Parameters and Procedures of High- and Low-Level Laser Therapy in Medical Research Articles - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC12515686/
4. Shining light on the head: Photobiomodulation for brain disorders - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC5066074/
5. Light buckets and laser beams: mechanisms and applications of ..., consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC12181550/
6. Under the spotlight: mechanisms of photobiomodulation concentrating on blue and green light - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC6685747/
7. Proposed Mechanisms of Photobiomodulation or Low-Level Light Therapy - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC5215870/
8. Photobiomodulation of Cytochrome c Oxidase by Chronic Transcranial Laser in Young and Aged Brains - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8971717/
9. Photobiomodulation—Underlying Mechanism and Clinical ..., consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC7356229/
10. Photobiomodulation for Neurodegenerative Diseases: A Scoping Review - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10855709/
11. Photomodulation alleviates cellular senescence of aging adipose-derived stem cells - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10278352/
12. Shedding Light on Photobiomodulation Therapy for Age-Related Macular Degeneration: A Narrative Review - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10640464/
13. Photobiomodulation has rejuvenating effects on aged bone marrow mesenchymal stem cells - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8219765/
14. Mechanisms and applications of the anti-inflammatory effects of photobiomodulation - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC5523874/
15. The Molecular Mechanisms of Action of Photobiomodulation Against Neurodegenerative Diseases: A Systematic Review - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8942959/
16. Mechanisms and Mitochondrial Redox Signaling in ... - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC5844808/
17. Inflammaging and Oxidative Stress in Human Diseases: From Molecular Mechanisms to Novel Treatments - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC6769561/
18. A comprehensive review on modulation of SIRT1 signaling pathways in the immune system of COVID‐19 patients by phytotherapeutic melatonin and epigallocatechin‐3‐gallate - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC9347991/
19. Activation of PKA/SIRT1 signaling pathway by photobiomodulation therapy reduces Aβ levels in Alzheimer's disease models - PubMed, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/31663252/
20. Oxidative stress is involved in LLLT mechanism of action on skin healing in rats - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8075128/
21. Photobiomodulation Activates Coordinated Signaling Networks to ..., consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC12785302/
22. Inflammation and aging-related disease: A transdisciplinary inflammaging framework - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC11872841/
23. The Mechanisms and Efficacy of Photobiomodulation Therapy for Arthritis: A Comprehensive Review - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10531845/
24. Inflammageing: chronic inflammation in ageing, cardiovascular disease, and frailty - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC6146930/
25. Experimental and Clinical Applications of Red and Near-Infrared Photobiomodulation on Endothelial Dysfunction: A Review - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC7998572/
26. SASP Modulation for Cellular Rejuvenation and Tissue ... - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC12025513/
27. Understanding cellular senescence: pathways involved, therapeutics and longevity aiding, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10730163/
28. The Senescence-Associated Secretory Phenotype (SASP) in the Challenging Future of Cancer Therapy and Age-Related Diseases - PubMed, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/33371508/
29. Characterization of Human Senescent Cell Biomarkers for Clinical Trials - PubMed - NIH, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/39823170/
30. Photobiomodulation with 590 nm Wavelength Delays the Telomere Shortening and Replicative Senescence of Human Dermal Fibroblasts In Vitro - PubMed, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/33090930/
31. Inflammatory markers and physical frailty: towards clinical application - PMC - NIH, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10770917/
32. Inflammaging markers characteristic of advanced age show similar levels with frailty and dependency - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC7902838/
33. Telomerase gene therapy ameliorates the effects of neurodegeneration associated to short telomeres in mice - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC6555470/
34. Telomere dysfunction induces sirtuin repression that drives telomere-dependent disease - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC6657508/
35. Low-power infrared laser modulates telomere length in heart tissue ..., consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC8131880/
36. SIRT1 regulates the localization and stability of telomerase protein by direct interaction, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/38749190
37. SIRT1 Acts as a Nutrient-sensitive Growth Suppressor and Its Loss Is Associated with Increased AMPK and Telomerase Activity - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC2262963/
38. The potential role of the SIRT1-Nrf2 signaling pathway in alleviating hidden hearing loss via antioxidant stress - PubMed, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/39618038/
39. Telomeres and SIRT1 as Biomarkers of Gamete Oxidative Stress, Fertility, and Potential IVF Outcome - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC11354255/
40. Photobiomodulation therapy (red/NIR LEDs) reduced the length of stay in intensive care unit and improved muscle function: A randomized, triple-blind, and sham-controlled trial - PubMed, consulté le février 20, 2026, https://pubmed.ncbi.nlm.nih.gov/38262071/
41. Evaluation of Efficacy of Low-Level Laser Therapy - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC7736953/
42. High-Intensity Vs. High-Power Laser Therapy: Biophysical Implications Of A Semantic Ambiguity - Preprints.org, consulté le février 20, 2026, https://www.preprints.org/manuscript/202511.0456/v1/download
43. High-Intensity vs. High-Power Laser Therapy: Biophysical ... - MDPI, consulté le février 20, 2026, https://www.mdpi.com/2076-3417/16/1/67
44. Photothermal Effects of High-Energy Photobiomodulation Therapies: An In Vitro Investigation - PMC, consulté le février 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC10295700/










Distributeur France Exclusif REYU
Distributeur Officiel France MILTA
Médecine douce naturelle et fonctionnelle –Technologies non invasives de régénération cellulaire REYU & MILTA
© 2025 Positive Life Equipements — Tous droits réservés
Accueil





